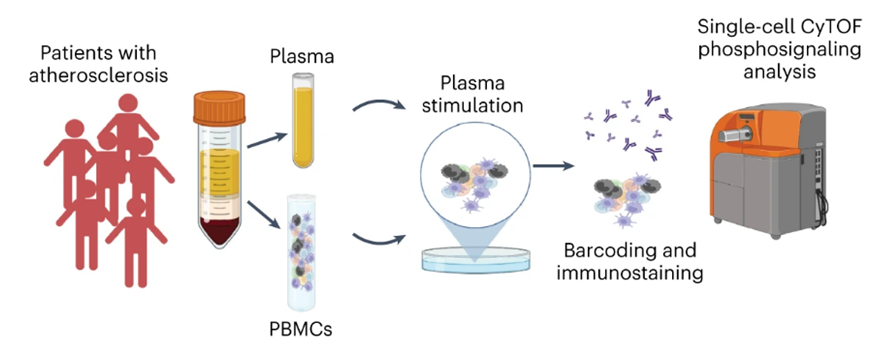
接着,研究者再次通过多参数质谱流式探究了暴露在动脉粥样硬化患者血浆中的健康免疫细胞内的信号传导,同时检测了细胞因子表达谱。结果显示,动脉粥样硬化病人的血浆可以影响健康细胞的炎症反应应答,其中CD14+ 单核细胞和 CD1c+树突状细胞展现出了最强的免疫激活功能,引起多种蛋白(CREB, p38, ERK1/2, MAPKAPK2 and S6)磷酸化。
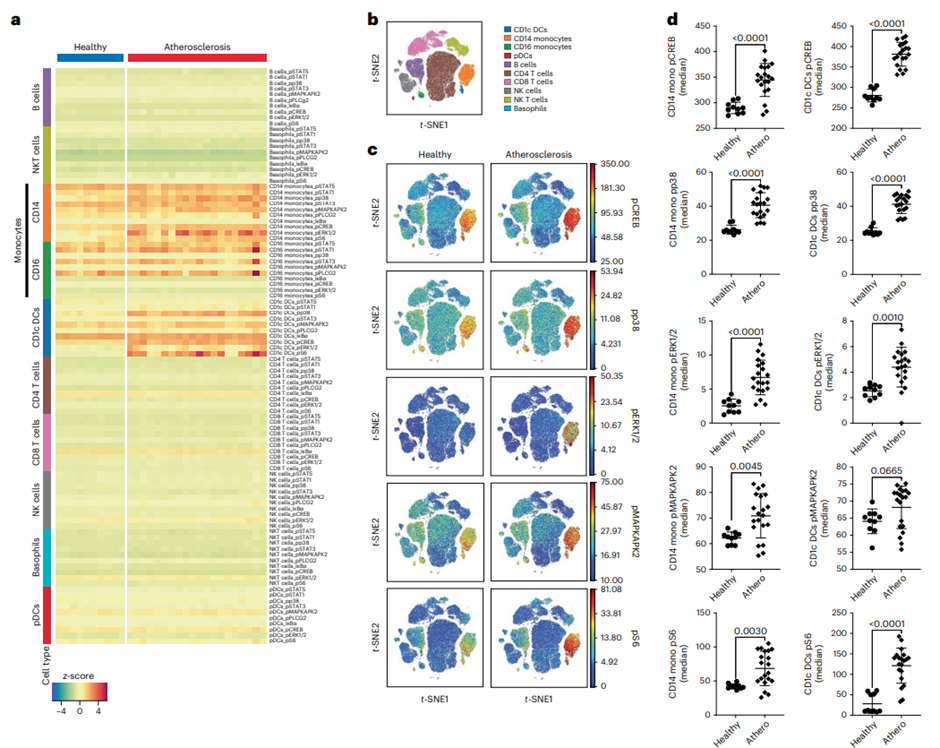
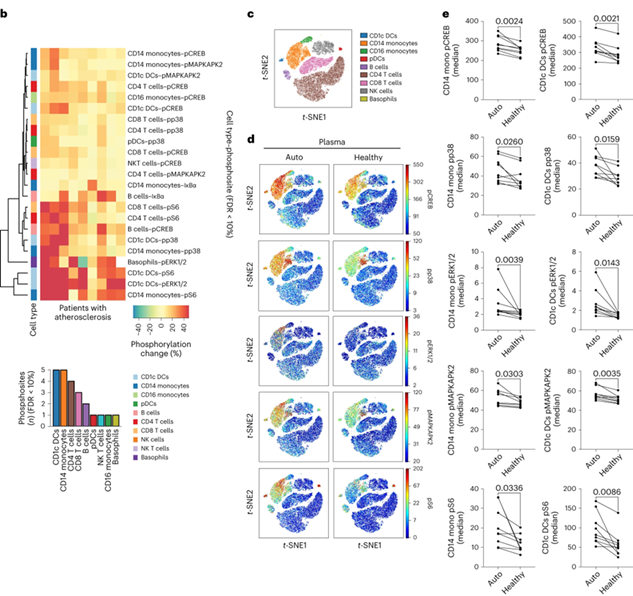
图3. 多参数质谱流式检测健康免疫细胞在动脉粥样硬化病人血浆刺激下的胞内信号
a: 健康免疫细胞在动脉粥样硬化病人血浆或健康人血浆刺激下的免疫细胞热图; b: 健康人主要PBMC细胞分群t-SNE图; c: 健康免疫细胞在动脉粥样硬化病人血浆或健康人血浆刺激下的胞内信号模式t-SNE图; d: 健康免疫细胞在自体血浆或健康人血浆刺激下CD14+ 单核细胞和 CD1c+ 树突状细胞的胞内激酶的磷酸化情况
而后,研究者通过质谱流式探究了动脉粥样硬化患者和健康供体的PBMC中存在的不同的静息和刺激免疫反应。以上结果表明,尽管动脉粥样硬化患者和健康供体的循环免疫细胞在基线时的炎症信号和健康血浆刺激下的炎症反应存在一定差异,但面对患者血浆的刺激,健康供体和动脉粥样硬化患者的PBMC具有相似的炎症反应,而动脉粥样硬化患者具有更强的循环免疫细胞炎症反应应答主要是由于与其自身血浆反应。
研究者设计了一种药物再利用的方法,深入分析了4823个基因,其中包括277个已知在炎症过程中扮演关键作用并能产生细胞因子和促进机体慢性炎性反应的蛋白质,该预测方法从L1000化合物筛选文库中发现现有的小分子以逆转对动脉粥样硬化血浆的炎症反应,药物筛选基于磷酸化CyTOF筛选、基因表达分析以及健康PBMC中存在或不存在候选药物时PBMC和斑块对动脉粥样硬化血浆的细胞因子分泌的综合分析。
通过该方法,研究者筛选出8个候选药物,其中通过质谱流式检测多种磷酸化蛋白后发现塞卡替尼对动脉粥样硬化患者血浆诱导的大多数特异性激酶和TF磷酸化有显著的抑制作用。为了进一步阐明塞卡替尼如何改变动脉粥样硬化斑块诱导的信号传导,研究者进行了进一步的磷酸化CyTOF实验来研究LCK、SRC和AKT,并证实动脉粥样硬化斑块增加了SRC和AKT的蛋白表达及其在CD14+单核细胞中的磷酸化,且无论动脉粥样硬化影响的血管部位如何,塞卡替尼都具有抗炎作用。总的来说,这些结果表明,塞卡替尼不仅对循环免疫细胞具有抗炎和抗动脉粥样硬化作用,而且直接对人类动脉粥样硬化组织具有一定作用。
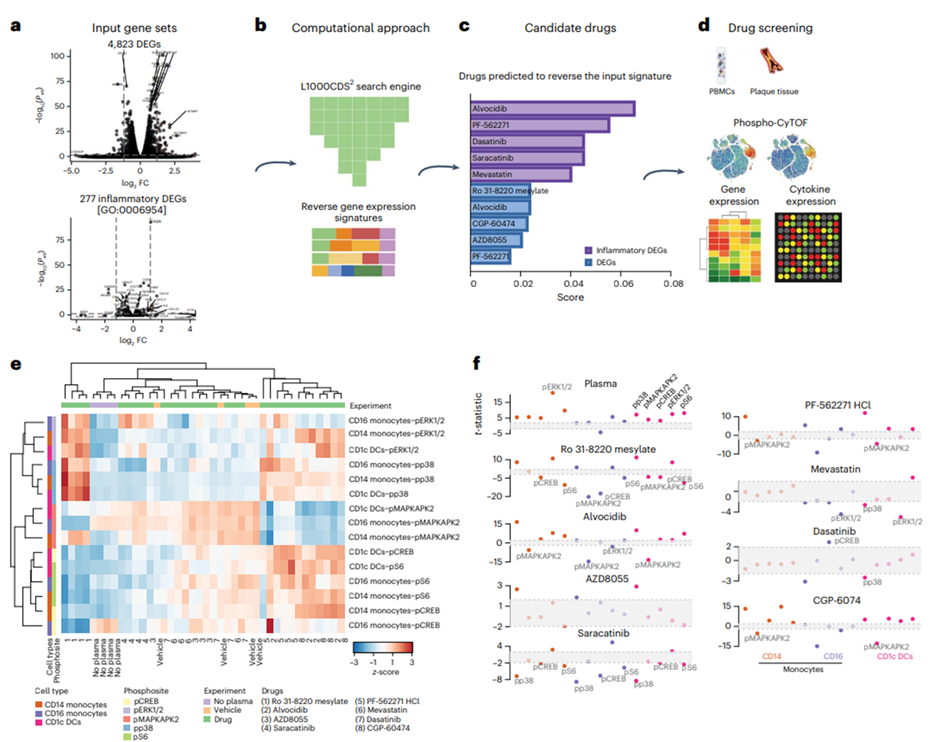
图4. 候选药物的磷酸化CyTOF检测
a-d:识别动脉粥样硬化疾病和离体的候选抗炎小分子的筛选方法流程图; e: CyTOF检测不同免疫细胞在单独动脉粥样硬化病人血浆以及配合不同候选药物处理下的单细胞磷酸化热图; f:单细胞和树突状细胞磷酸化情况的t-统计分析
最后,通过质谱流式分析检测了小鼠模型的循环免疫细胞,探究了塞卡替尼在动物动脉粥样硬化模型中也能发挥抗动脉粥样硬化和抗炎作用。
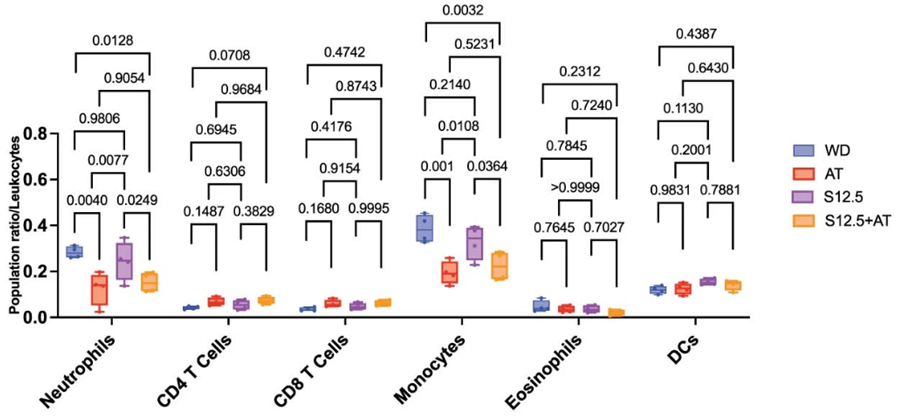
图5. 动物模型中的质谱流式检测
CyTOF分析对照组以及不同处理下的16周小鼠全血中的循环免疫细胞组成
在本研究中,研究人员并未尝试耗费大量时间和资金从头开发一种合适的药物,而是转而分析一份已经获批或用于其它用途的候选药物清单,通过质谱流式检测技术,单细胞测序技术等从候选清单中筛选出塞卡替尼,并评估塞卡替尼在动脉粥样硬化中的抗炎作用。本研究所采用的这种系统免疫学驱动药物的重定向与临床前的验证策略,有助于人类心血管疾病免疫疗法的开发,也为抗炎药物新用途的探索提供新思路。
参考文献:
Amadori, L., Calcagno, C., Fernandez, D.M. et al. Systems immunology-based drug repurposing framework to target inflammation in atherosclerosis. Nat Cardiovasc Res (2023). doi:10.1038/s44161-023-00278-y