三阴性乳腺癌(TNBC)指雌激素受体(ER)、孕激素受体(PR)和人表皮生长因子受体2(HER2)三者免疫组织化学染色结果均为阴性的乳腺癌,被称为“最毒乳腺癌”。传统的内分泌治疗和HER2靶向治疗对TNBC患者治疗效果不佳,而程序性死亡蛋白1(PD-1)和程序性细胞死亡配体1(PD-L1) 作用的免疫检查点阻断疗法(ICB)能够使部分TNBC患者获益,但目前缺乏可靠的生物标志物来识别应答者。
尽管多细胞组织预处理可能表明ICB是否可以增强免疫应答反应,但ICB如何重塑组织结构以实现这一点仍然模糊不清,在治疗期间的组织动态与免疫应答之间的关系尚不清楚。
为了回答这个问题,剑桥大学Raza Ali团队以及意大利San Raffaele医院Giampaolo Bianchini课题组在新辅助疗法的随机试验中,使用组织成像质谱流式(Imaging mass cytometry, IMC)精确量化了患者肿瘤中采样的三个时间点的细胞的表型、活化状态和空间位置与TNBC免疫治疗的应答。研究论文发表在《Nature》上,题为“Spatial predictors of immunotherapy response in triple-negative breast cancer”,通过绘制TNBC原位多细胞肿瘤生态系统图,发现了关键的ICB 反应预测因子,并表明 ICB 能明显重塑肿瘤结构。

作者在三个时间点取样(基线,n= 243;治疗早期,n= 207;治疗后,n= 210),采用IMC技术对43种蛋白质进行单细胞蛋白表达和空间分布的分析,获得共1855张高维组织图像,用于后续数据分析。这些FFPE样本来自于NeoTRIP 三期临床对照试验,通过1:1随机比较了新辅助化疗(卡铂和白蛋白结合型紫杉醇)与化疗联合抗PD-L1免疫疗法(卡铂、白蛋白结合型紫杉醇和阿替利珠单抗)。
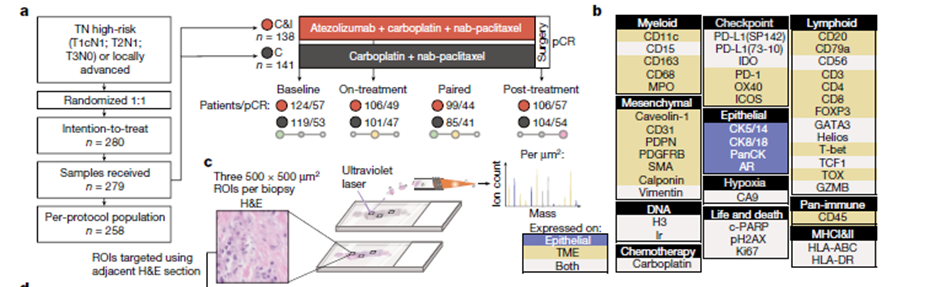
图1a. NeoTRIP免疫疗法试验的IMC工作流程
图1b. IMC检测43种蛋白列表
精准定义细胞表型:使用深度学习分离上皮细胞(癌细胞)和TME细胞,聚类得到17种上皮表型和20种TME表型。
【癌症-免疫相互作用预测ICB的应答效应】
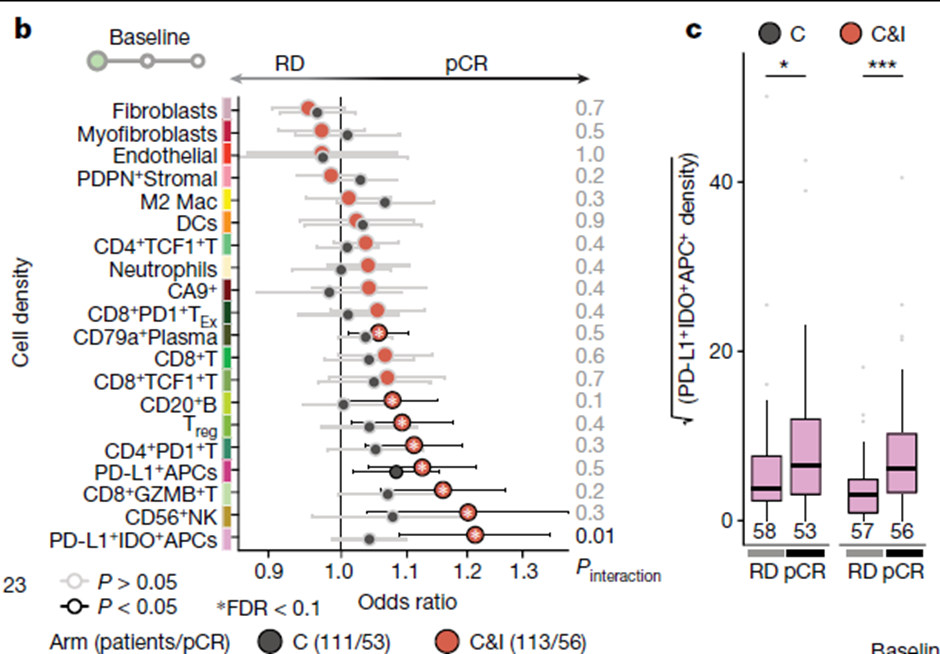
图2b. 基线期的免疫疗法响应空间预测因子PDL1+IDO+APC;
图2c 不同治疗组对应PDL1+IDO+APC密度
首先,作者探索了不同上皮和肿瘤微环境细胞表型的密度是否在预测响应方面存在差异,发现只有PDL1+IDO+APC密度可以预测ICB的响应(图2b-c)。紧接着,研究不同的细胞-细胞相互作用是否与免疫治疗的反应相关,结果发现,上皮-CD20+B(Pinteraction = 0.003,FDR = 0.06)和上皮-CD8+GZMB+T(Pinteraction = 0.006,FDR = 0.06)细胞交互显示最大的差异效应。TME细胞则没有发现差异反应的显著预测因子。通过对接触癌细胞的T细胞进行分析,发现其更会增殖的关键活化标记物。以上这些发现证实了细胞-细胞相互作用的功能意义。
【增殖评分预测ICB的应答效应】
与癌细胞接触的T细胞更常是Ki67+,也与ICB反应中的增殖有关。作者计算了每个表型中Ki67+细胞的比例(增殖评分),并测试了其与pCR的相关性。
图3b. 不同肿瘤增殖评分与免疫治疗反应的统计
图3c. 不同TME细胞类型与免疫治疗反应的统计
结果显示,当患者接受免疫治疗时,共计12种上皮细胞和16种TME细胞表型预测应答(图3b-c)。MHCI&IIhi细胞的增殖评分是上皮(癌症)细胞免疫治疗反应的最强预测因子,而CD8+ TCF1+ T细胞是整体上最强的免疫治疗反应预测因子。然而,MHCI&IIhi癌细胞和CD8+ TCF1+ T细胞的增殖分数仅呈中度相关(ρ = 0.46)。值得注意的是,CD8+ TCF1+ T细胞是一种干细胞样群体,它是ICB诱导的增殖发生的基础。总体结论是,治疗前的增殖评分富集了处于不同激活状态的细胞,并识别了预测ICB反应的表型。
【治疗后的ICB响应预测因子】
作者还研究了治疗早期的细胞密度、细胞-细胞相互作用和免疫治疗反应之间的联系。
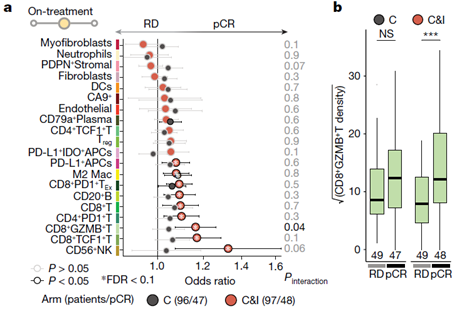
治疗早期免疫响应的细胞表型预测:图4a,上皮细胞表型密度与pCR之间的比值比,图4b,各治疗组CD8+GZMB+T上皮细胞密度和治疗反应的关系
TME细胞密度中只有CD8+GZMB+T细胞显示显著差异免疫治疗反应预测(Pinteraction =0.04,FDR=0.5,图4a-b),为同型细胞相互作用。在一些ICB耐药的病例中,癌细胞中CD15的表达具有显著的高表达模式。我们还观察到CD15+癌细胞灶被CD15+白细胞包围,这表明异型相互作用可能是状态转变的驱动因素。对免疫治疗应答的特征是CD8+ GZMB+ T细胞的积累,而异型CD79a+浆细胞相互作用和CD15+癌细胞意味着耐药肿瘤。
【ICB免疫应答的细胞动态变化】
与基线相比,我们发现了治疗时免疫治疗响应的不同驱动因素,促使作者研究了新辅助免疫治疗的细胞动态变化。免疫细胞在治疗早期显著增加,而在治疗后显著减少,同时上皮(癌症)细胞减少,基质细胞增加(图5a)。这种模式在所有组中都重复了,但变化的程度不同:在应答者中免疫细胞早期比例的增加更大,而在接受免疫治疗的应答者中最大。
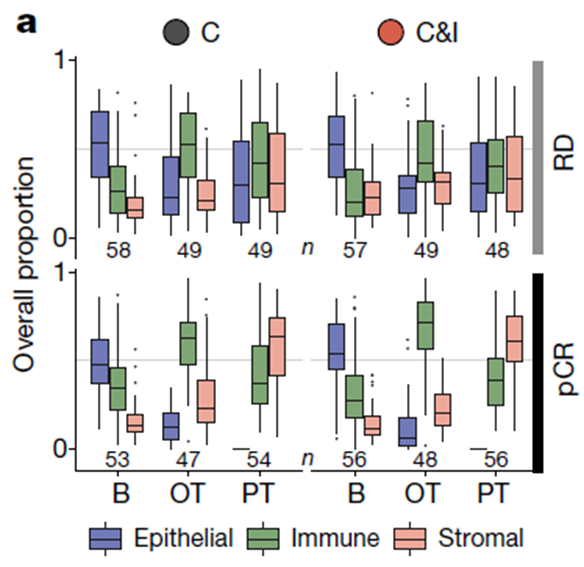
图5a. 免疫治疗的细胞动态变化
【主要的ICB应答预测因子】
作者获得了148个组织特征(37个细胞表型的密度;37个异型和37个同型细胞-细胞相互作用;37个增殖评分),并发现其比化疗反应更能预测免疫治疗。
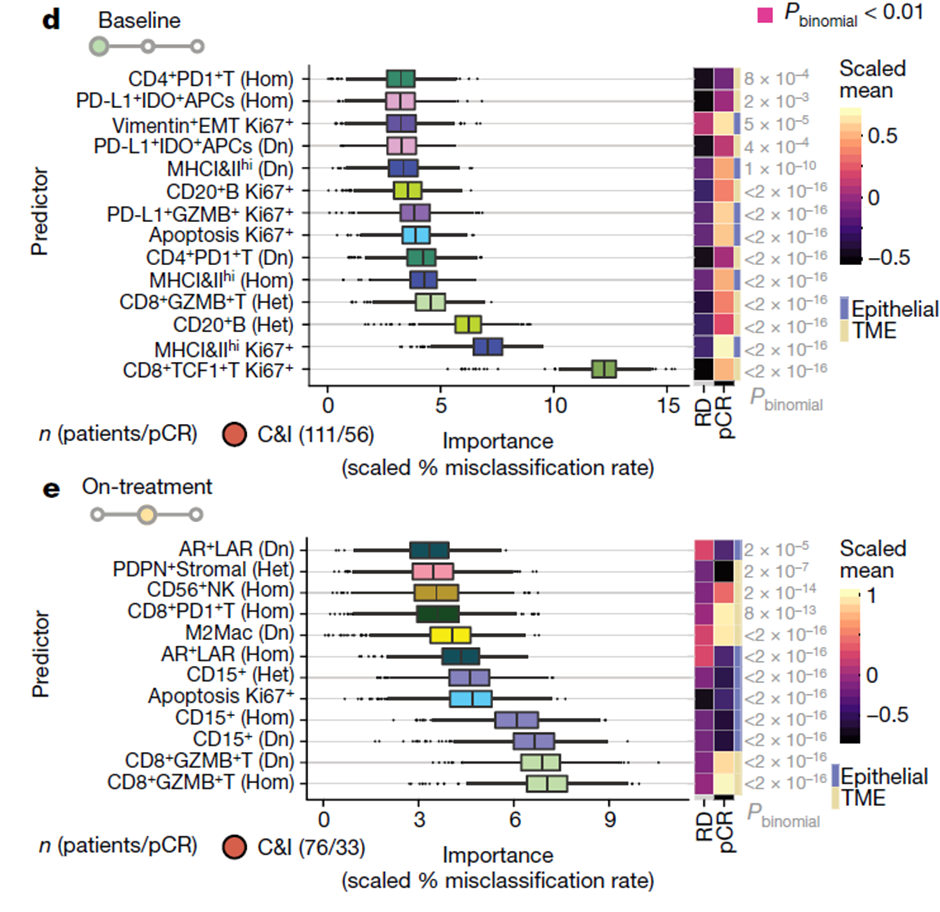
图6. 预测ICB响应的多变量模型,免疫治疗反应的基线(d)和治疗中(e)预测因子在模型中的重要性排序
总的来说,增殖的CF1T+ CD8+ T细胞和MHCII+ 癌细胞的分数是免疫应答的主要预测因子,其次是与B细胞和GZMB+ T细胞的癌症免疫相互作用。在治疗过程中,反应性肿瘤含有丰富的GZMB+ T细胞,而耐药肿瘤则以CD15+ 癌细胞为特征。通过结合治疗前和治疗中的组织特征,可以最好地预测应答,指出早期活检在指导适应性治疗中的作用。
该研究表明,多细胞空间组织分布是三阴性乳腺癌ICB疗效的主要决定因素,并提示原位系统分析肿瘤微环境细胞分布将有助于实现肿瘤精准免疫治疗。
组织成像质谱分析系统采用金属标签,帮助客户顺利开展43种蛋白的分析,具有实验设计简便、实验结果可靠的特点,其完整的解决方案为三阴性乳腺癌肿瘤组织与TME组织的原位空间分布提供了全面的视角,帮助用户实现对不同阶段样本的细胞组成和功能进行挖掘,进而一窥ICB重塑细胞组织结构的过程。
参考文献:
Wang, X.Q., Danenberg, E., Huang, C.S., Egle, D., Callari, M., Bermejo, B., Dugo, M., Zamagni, C., Thill, M., Anton, A. and Zambelli, S., 2023. Spatial predictors of immunotherapy response in triple-negative breast cancer. Nature, 621(7980), pp.868-876.












